ニュースリリース
ニュースリリース

2026.03.25
世界の舞台で「夢に向かって打て!」新TVCM「リポビタンDays×松山英樹選手 篇」公開

2026.03.19
リポビタンDチャレンジカップ2026 ラグビー日本代表戦の追加協賛が決定

2026.03.16
「ヴイックス すっきり甘くないのど飴」 個包装タイプになってリニューアル発売!!

2026.03.06
「最強レベル」美白UVのビッグサイズが、今年も数量限定販売開始!

2026.03.02
第27回全国高等学校選抜ラグビーフットボール大会に協賛決定
2026.03.02
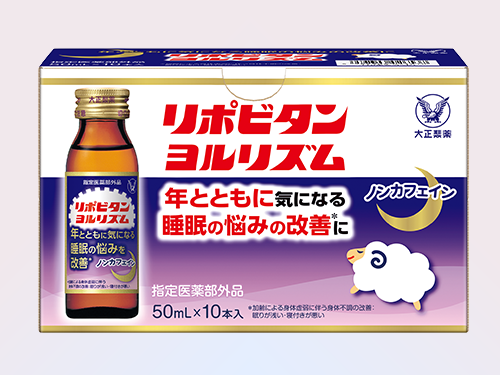
大正製薬独自の処方設計で、加齢に伴う睡眠の悩みを改善「リポビタンヨルリズム」新発売!!
2026.02.26
休止期脱毛症に 発毛成分「ミノキシジル」が有用な可能性を見出す

2026.02.20
大正製薬株式会社 会社人事

2026.02.12
「子どもたちのみらいのために 未来応援プロジェクト2025」寄付決定のお知らせ

2026.02.10
大正製薬株式会社 会社人事

2026.02.02
リポビタンDチャレンジカップ2026 ラグビー日本代表戦に特別協賛、冠スポンサーに決定

2026.01.06